替雷利珠单抗(Tislelizumab)是一种免疫类靶向药物,常用于治疗多种实体肿瘤,能够一定程度延长患者生存期、改善预后。目前替雷利珠单抗已经在国内上市,本文就替雷利珠单抗的适应症、用法用量、副作用、禁忌、临床疗效等进行了详细说明。
(一)适应症
替雷利珠单抗(Tislelizumab)作为单药,适用于既往全身化疗后未含PD-(L)1抑制剂的不可切除或转移性食管鳞状细胞癌成人患者的治疗。
替雷利珠单抗
(二)用法用量
1.推荐剂量
替雷利珠单抗的推荐剂量为200mg,每3周静脉输注一次,直到疾病进展或不可接受的毒性。
第一次输注需超过60分钟。如果患者耐受,后续输注可超过30分钟。
2.不良反应的剂量调整
不建议减少替雷利珠单抗的剂量。一般情况下,对于严重的(3级)免疫介导的不良反应,应停用替雷利珠单抗。对于危及生命的(4级)免疫介导的不良反应,复发性严重(3级)免疫介导的反应,需要全身免疫抑制治疗,或在开始类固醇治疗的12周内将皮质类固醇剂量减少到每天10mg或更少的泼尼松剂量。
表1总结了替雷利珠单抗针对不同于一般指南管理的不良反应的剂量调整。
表1:不良反应的推荐剂量调整
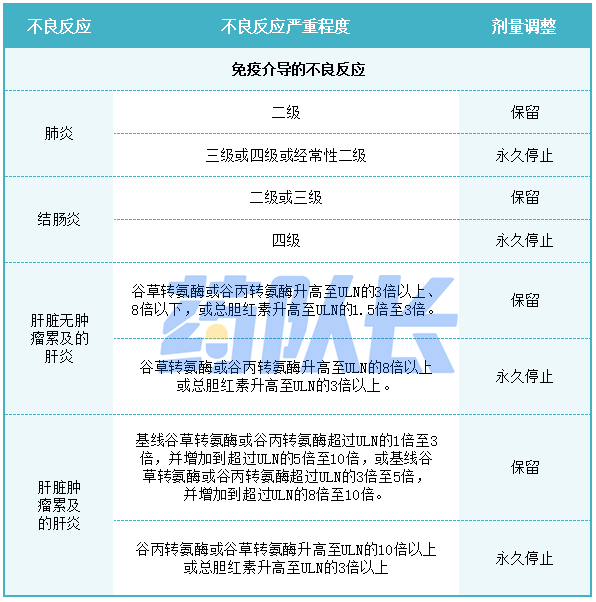
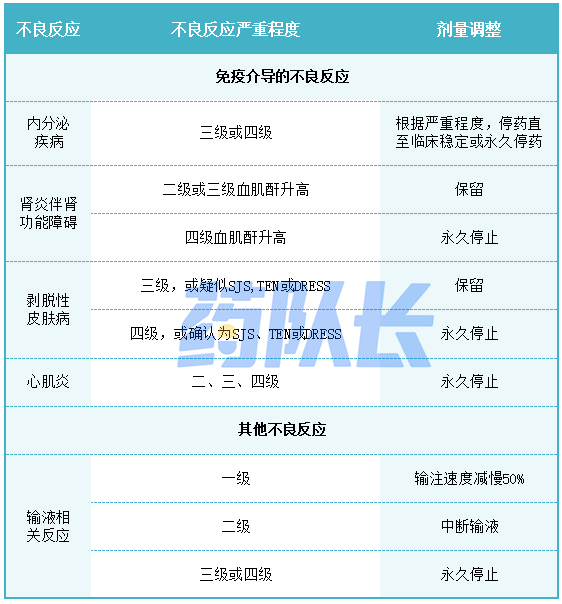
3.准备和管理
(1)准备
在溶液和容器允许的情况下,注射用药品在给药前应目视检查是否有颗粒物质和变色。替雷利珠单抗是一种透明至微乳白色,无色至微黄色溶液。如果溶液混浊、变色或含有可见颗粒,请丢弃小瓶。不要摇晃药瓶。
按如下方法配制输注溶液
从两瓶100mg替雷利珠单抗中取出20mL替雷利珠单抗(20mL中总共200mg)。
将溶液转移到含有0.9%氯化钠注射液(USP)的静脉(IV)输液袋中,制备终浓度在2mg/mL至5mg/mL之间的输液。
将稀释后的溶液温和倒置混合,以避免溶液起泡或过度剪切。不要摇晃。
替雷利珠单抗仅限一次性使用,使用后需丢弃瓶中剩余的未使用的部分。替雷利珠单抗不含任何防腐剂。
将替雷利珠单抗稀释后的溶液保存
从稀释后开始在室温下放置保存不超过4小时。这包括稀释溶液的室温储存和输注持续时间。
在2°C至8°C(36°F至46°F)下冷藏不超过20小时。如果冷藏,在给药前将稀释后的溶液放至室温。
在室温下放置4小时或冷藏20小时后丢弃稀释后的溶液。不要冷冻稀释后的溶液。
(2)管理
将稀释后的溶液通过静脉输注,静脉输注使用无菌的、无热原的、低蛋白结合的0.2μm或0.22μm的在线过滤器或附加过滤器。
首次输注应在60分钟内完成。如果患者耐受,所有后续的输注可以在30分钟内进行。
不要通过同一输液线同时给药其他药物。
不要静脉推注或单次注射替雷利珠单抗。
输液结束时必须冲洗静脉导管。
(三)适用人群
成人。妊娠期、哺乳期女性,儿童以及老年患者在医生指导下用药。
(四)禁忌症
尚不明确。
(五)副作用
包括替雷利珠单抗实验室异常在内的最常见不良反应(≥20%)为:葡萄糖升高、血红蛋白降低、淋巴细胞减少、钠减少、白蛋白减少、碱性磷酸酶增加、贫血、疲劳、谷丙转氨酶增加、肌肉骨骼疼痛、体重减轻、谷丙转氨酶增加和咳嗽。
(六)注意事项
1.严重和致命的免疫介导不良反应
(1)免疫介导的肺炎
替雷利珠单抗可引起免疫介导性肺炎,这可能是致命的。在接受其他PD-1/PDL1阻断抗体治疗的患者中,先前接受过胸部放疗的患者的肺炎发病率更高。
(2)免疫介导性结肠炎
替雷利珠单抗可引起免疫介导性结肠炎,这可能是致命的。在使用PD-1/PD-L1阻断抗体治疗的皮质类固醇难治性免疫介导性结肠炎患者中有巨细胞病毒(CMV)感染/再激活的报道。在皮质类固醇难治性结肠炎的病例中,考虑重复感染性检查以排除其他病因。
(3)免疫介导性肝炎
替雷利珠单抗可引起免疫介导性肝炎,这可能是致命的。接受替雷利珠单抗治疗的患者中,免疫介导性肝炎发生率为1.7%(34/1972),包括致死性(0.1%)、4级(0.1%)、3级(1%)和2级(0.6%)不良反应。
(4)免疫介导性内分泌疾病
肾上腺机能不全
替雷利珠单抗可引起免疫介导的肾上腺功能不全。对于2级或以上的肾上腺功能不全,开始对症治疗,包括临床指征的激素替代。根据严重程度停用替雷利珠单抗。
下垂体炎
替雷利珠单抗可引起免疫介导性垂体炎。垂体炎可表现为与肿块效应相关的急性症状,如头痛、畏光或视野缺损。垂体炎可引起垂体功能减退。
根据临床指示启动激素替代。根据严重程度,暂停或永久停用替雷利珠单抗。
甲状腺疾病
替雷利珠单抗可引起免疫介导的甲状腺疾病。甲状腺炎可伴有或不伴有内分泌病变。
甲状腺功能亢进可继发甲状腺功能减退。启动激素替代甲状腺功能减退或机构医疗管理甲状腺机能亢进的临床指征。根据严重程度,暂停或永久停用替雷利珠单抗。
1型糖尿病,可伴有糖尿病酮症酸中毒
1型糖尿病有PD-1/PD-L1阻断抗体的报道。监测患者是否有高血糖或其他糖尿病体征和症状。根据临床需要开始胰岛素治疗。
根据严重程度,暂停或永久停用替雷利珠单抗。
(5)免疫介导的肾炎伴肾功能不全
替雷利珠单抗可引起免疫介导性肾炎,这可能是致命的。根据严重程度,暂停或永久停用替雷利珠单抗。
(6)免疫介导的皮肤不良反应
替雷利珠单抗可引起免疫介导的皮疹或皮炎。严重皮肤不良反应(scar)的病例,包括剥脱性皮炎、史蒂文斯-约翰逊综合征(SJS)和中毒性表皮坏死松解(TEN),已被报道,其中一些有致命的结果。局部润肤剂和/或局部皮质类固醇可能足以治疗轻度至中度非剥脱性皮疹。根据严重程度,暂停或永久停用替雷利珠单抗。
(7)其他免疫介导的不良反应
在1972年接受替雷利珠单抗治疗的患者中,以下临床显著的免疫介导不良反应发生率均低于1%:肌炎、心肌炎、关节炎、风湿性多肌痛和心包炎。其他PD-1/PD-L1阻断抗体还报道了以下临床显著的免疫介导不良反应,包括严重或致命的病例。
心脏/血管:血管炎
神经系统
脑膜炎、脑炎、脊髓炎和脱髓鞘、重症肌无力综合征/重症肌无力(包括加重)、格林-巴利综合征、神经麻痹、自身免疫性神经病变。眼部:可发生葡萄膜炎、虹膜炎和其他眼部炎症毒性。有些病例可伴有视网膜脱离。可能出现不同程度的视力损害,包括失明。如果葡萄膜炎合并其他免疫介导的不良反应,考虑vogt-koyanagi-harada样综合征,因为这可能需要全身性类固醇治疗以降低永久性视力丧失的风险。
眼部
可能出现葡萄膜炎、虹膜炎和其他眼部炎症毒性。有些病例可能与视网膜脱离有关。可能出现各种程度的视力障碍,包括失明。如果葡萄膜炎合并其他免疫介导的不良反应,医生需要考虑ogt-小柳-原田样综合征,因为这可能需要全身性类周醇治疗以降低永久性视力丧失的风险。
胃肠
胰腺炎,包括血清淀粉酶和脂肪酶水平升高、胃炎、十二指肠炎。
肌肉骨骼和结缔组织
多发性肌炎、横纹肌溶解症及相关后遗症,包括肾衰竭。
内分泌
甲状旁腺功能减退。
其他(血液/免疫)
溶血性贫血、再生障碍性贫血、噬血细胞性淋巴组织细胞增多症、全身炎症反应综合征、组织细胞坏死性淋巴结炎(池池淋巴结炎)、结节病、免疫性血小板减少性紫癜、实体器官移植排斥反应、其他移植(包括角膜移植)排斥反应。
2.输注相关反应
替雷利珠单抗可引起严重或危及生命的输液相关反应。4.2%(83/1972)接受替雷利珠单抗的患者发生输注相关反应,包括3级或以上(0.3%)反应。监测患者输注相关反应的体征和症状。
对于轻度(1级)输液反应减慢输液速度,对于中度(2级)输液相关反应中断输液。对于严重(3级)或危及生命(4级)的输注相关反应,应停止输注并永久停用替雷利珠单抗。
3.异体造血干细胞移植的并发症
在接受PD-1/PD-L1阻断抗体治疗之前或之后接受同种异体造血干细胞移植(HSCT)的患者可能发生致命和其他严重并发症。移植相关并发症包括超急性移植物抗宿主病(GVHD)、急性移植物抗宿主病、慢性移植物抗宿主病、低强度调节后的肝静脉闭塞性疾病和需要类固醇的发热综合征(没有确定的感染原因)。尽管在PD-1/PD-L1阻断和异体造血干细胞移植之间进行干预治疗,这些并发症仍可能发生。
密切跟踪患者是否有移植相关并发症,并及时干预。考虑在异体造血干细胞移植之前或之后使用PD-1/PD-L1阻断抗体治疗的获益与风险。
4.胚胎-胎儿毒性
根据其作用机制,替雷利珠单抗在给孕妇使用时可能会对胎儿造成伤害。建议妇女注意对胎儿的潜在风险。建议有生殖潜力的女性在替雷利珠单抗治疗期间和最后一次给药后4个月内采取有效避孕措施。
(七)治疗效果
1.试验设计
这是一项开放标签的III期临床研究,纳入了512名晚期或转移性食管鳞状细胞癌(ESCC)患者。
2.试验结果的设定
患者被随机分配接受静脉注射替雷利珠单抗(一种抗程序性细胞死亡药物)蛋白1抗体,每3周200mg或化疗(研究者选择紫杉醇、多西紫杉醇或伊立替康)。主要终点是所有患者的总生存期(OS)。
3.试验结果
在所有患者中,与化疗相比,替雷利珠单抗治疗具有更高的客观缓解率(20.3%vs9.8%)和更持久的抗肿瘤反应(中位时间为7.1个月vs4.0个月)。与化疗相比,替雷利珠单抗组发生≥3级治疗相关不良事件的患者较少。化疗作为二线治疗晚期或转移性ESCC患者相比,替雷利珠单抗显着改善OS,且安全性尚可。与化疗相比,程序性死亡配体1TAP≥10%的患者也表现出替雷利珠单抗具有统计学上显着的生存获益。
(八)药物相互作用
尚不明确。
(九)储存条件
请置于原包装盒内的冰箱中,避光保存,温度为2'C至8°C(36°F至46°F),不要冷冻,不要摇晃。
【温馨提示】:部分商品说明书更换频繁,请以商品实物为准。

- 【宫颈癌】ZG005[适 应 症]一线标准治疗失败的晚期宫颈癌[试验分期]Ⅰ期
- 【BRAF突变实体瘤】双机制ERK1/2抑制剂GH55[适 应 症]BRAF突变实体瘤[试验分期]Ⅰ期
- 实体瘤|KH801注射液[适 应 症]复发/难治性或转移性晚期实体瘤患者[试验分期]Ⅰ期
- 初治胃癌|CLDN18.2单抗ASKB589联合化疗+免疫治疗[适 应 症]不可切除的局部晚期、复发性或转移性胃及食管胃交界处腺癌[试验分期]Ⅲ期
- 弥漫大B细胞淋巴瘤|盐酸米托蒽醌脂质体[适 应 症]复发性/难治性弥漫大B细胞淋巴瘤[试验分期]Ⅱ期
- 宫颈癌|PD-1/TIGIT双抗ZG005[适 应 症]至少经一线标准治疗失败(既往需要接受过含铂方案的化疗)的复发转移性宫颈癌[试验分期]Ⅰ期、Ⅱ期