叶酸α(FRα)受体可在正常细胞中低表达,在肿瘤细胞中高表达,使肿瘤细胞复制加快,更易产生治疗抗性,从而导致恶性肿瘤的预后更差。2022年,美国药监局(FDA)批准靶向FRα受体的ADC药物—ELAHERE(Mirvetuximab soravtansine)上市,适用于既往接受过1至3种全身治疗方案的FRα阳性、铂耐药上皮性卵巢癌、输卵管癌或原发性腹膜癌的成人患者。本文就ELAHERE治疗效果、安全性、治疗优势和上市信息等进行了详细描述。
FDA首个靶向叶酸α受体的ADC药物—ELAHERE上市
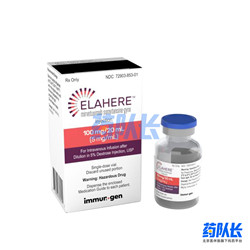
抗体药物偶联物(ADC)可将强效化疗的细胞杀伤力与抗体的选择性集于一体,近年来一直是药物研究的热点。2022年11月24日,美国药监局(FDA)传来喜讯,首个靶向叶酸α(FRα)受体的ADC药物—ELAHERE(Mirvetuximab soravtansine)获批上市。
FRα是最主要的叶酸受体(FR),通常在正常细胞中低表达,在肿瘤细胞中高表达。FRα阳性表达可使肿瘤细胞复制加快,更易产生治疗抗性,从而导致恶性肿瘤的预后更差。ELAHERE的获批,将为FRα阳性的上皮性卵巢癌、输卵管癌或原发性腹膜癌患者的治疗带来新的突破。
ELAHERE
ELAHERE靶向FRα受体有哪些治疗优势?
因FRα可在肿瘤组织中高表达且亲和力更高,ADC药物精准的靶向性使ELAHERE对正常组织的不良反应显著降低。
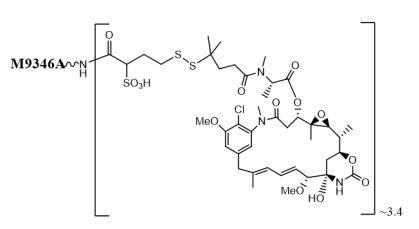
ELAHERE化学结构(图源于网络 侵权请告知)
有研究显示,在不表达FRα的组织中,ELAHERE作为叶酸复合体可快速经肾脏排除,但在表达FRα的肿瘤组织中,相较于抗体类药物仅能作用于毛细血管周围的肿瘤细胞,无法作用于远离毛细血管周围的肿瘤细胞,ELAHERE的渗透性极强且作用范围更广。此外,叶酸受体显像可帮助医生选择FRα表达阳性的患者,以便ELAHERE更好的发挥疗效。
71.4%FRα高表达上皮性卵巢癌患者肿瘤缩小,ELAHERE安全性良好
单药化疗对于铂耐药的上皮性卵巢癌患者的抗肿瘤活性有限且具有相当大的毒性,SORAYA研究评估了ELAHERE用于既往接受过包括贝伐珠单抗在内的1-3种治疗的,FRα高表达且铂耐药的上皮性卵巢癌患者的临床疗效和安全性。
中位随访13.4个月后,接受ELAHERE治疗的患者客观缓解率(ORR)为32.4%,其中5例达到完全缓解(CR),29例达到部分缓解(PR)。值得注意的是,接受ELAHERE治疗后有71.4%的患者肿瘤缩小,中位缓解持续时间(DOR)为6.9个月。安全性上,患者最常见的治疗相关的不良反应是视力模糊、角膜病变和恶心。
该研究证实,ELAHERE用于贝伐珠单抗经治的FRα高表达且铂耐药的上皮性卵巢癌患者表现出良好的抗肿瘤活性,以及可耐受的安全性。基于多项研究结果,FDA加速批准ELAHERE适用于既往接受过1至3种全身治疗方案的叶酸受体α(FRα)阳性、铂耐药上皮性卵巢癌、输卵管癌或原发性腹膜癌的成人患者,并且该药获得FDA“孤儿药”认定。
首款卵巢癌ADC药物,ELAHERE国内上市了吗?
自2014年以来,FDA无任何治疗铂耐药性卵巢癌的新药上市,ELAHERE打破了这一僵局,成为首款治疗铂耐药性卵巢癌的ADC药物。在另一项MIRASOL研究中,与医生选择的标准化疗相比,ELAHERE用于既往接受过贝伐珠单抗治疗且患有铂耐药的FRɑ高表达晚期高级上皮性卵巢癌、原发性腹膜癌或输卵管癌女性患者,无进展生存期(PFS)和总生存期(OS)分别延长了36%和26%。用于既往未接受过贝伐珠单抗治疗的女性患者,相较于医生选择的标准化疗,其无进展生存期提高了36%,总生存期延长了26%。
令人遗憾的是,目前该药尚未在中国上市,但ELAHERE研究仍未止步。ELAHERE已被证实在FRɑ高表达时最有效,有研究人员发现,当FRɑ表达水平中等或较低时,也具有一定的疗效,我们期待该结论能在未来的研究中得到更明确地验证,从而造福更多的肿瘤患者。

- 【宫颈癌】ZG005[适 应 症]一线标准治疗失败的晚期宫颈癌[试验分期]Ⅰ期
- 【BRAF突变实体瘤】双机制ERK1/2抑制剂GH55[适 应 症]BRAF突变实体瘤[试验分期]Ⅰ期
- 实体瘤|KH801注射液[适 应 症]复发/难治性或转移性晚期实体瘤患者[试验分期]Ⅰ期
- 初治胃癌|CLDN18.2单抗ASKB589联合化疗+免疫治疗[适 应 症]不可切除的局部晚期、复发性或转移性胃及食管胃交界处腺癌[试验分期]Ⅲ期
- 弥漫大B细胞淋巴瘤|盐酸米托蒽醌脂质体[适 应 症]复发性/难治性弥漫大B细胞淋巴瘤[试验分期]Ⅱ期
- 宫颈癌|PD-1/TIGIT双抗ZG005[适 应 症]至少经一线标准治疗失败(既往需要接受过含铂方案的化疗)的复发转移性宫颈癌[试验分期]Ⅰ期、Ⅱ期