曲贝替定作为一种抗肿瘤的化学药物,在既往接受过蒽环类药物治疗的不可切除或转移性脂肪肉瘤或平滑肌肉瘤的治疗中疗效显著,并且于2015年获得美国药监局FDA批准上市。本文就曲贝替定的用法用量进行了详细说明。
用法用量
1.推荐剂量
(1)推荐剂量为1.5mg/m2,每21天通过中心静脉输注一次,每次24小时,直至病情恶化或出现不可接受的毒性反应。
(2)中度肝功能损害患者(胆红素水平高于正常值上限的1.5倍至3倍,谷草转氨酶(AST)或谷丙转氨酶(ALT)低于正常值上限的8倍)的推荐剂量为0.9mg/m2。重度肝功能损害患者(胆红素水平高于正常值上限的3倍,且谷草转氨酶和谷丙转氨酶高于正常值上限的8倍)禁用曲贝替定。
2.药前治疗
每次服用曲贝替定前30分钟,静脉注射地塞米松20mg。
3.不良反应的剂量调整
以下情况永久停用曲贝替定:
(1)需要延迟给药超过3周的持续不良反应。
(2)肝功能正常的患者服用1.0mg/m2的曲贝替定后,或原有中度肝功能损害的患者服用0.3mg/m2的曲贝替定后,出现需要减量的不良反应。
(3)严重肝功能障碍:肝功能基线正常的患者,胆红素为正常值上限的2倍,谷草转氨酶或谷丙转氨酶为正常值上限的3倍,碱性磷酸酶低于前一治疗周期正常值上限的2倍。
(4)加重原有中度肝功能损害患者的肝功能异常。
(5)毛细血管渗漏综合征。
(6)横纹肌溶解症。
(7)提示心肌病的3级或4级心脏不良事件(AE),或射血分数 降至正常值下限以下的受试者。
针对不良反应的建议剂量调整方案见表1。一旦减少了曲贝替定的剂量,在随后的治疗周期中就不应再增加剂量。
表1:建议剂量调整
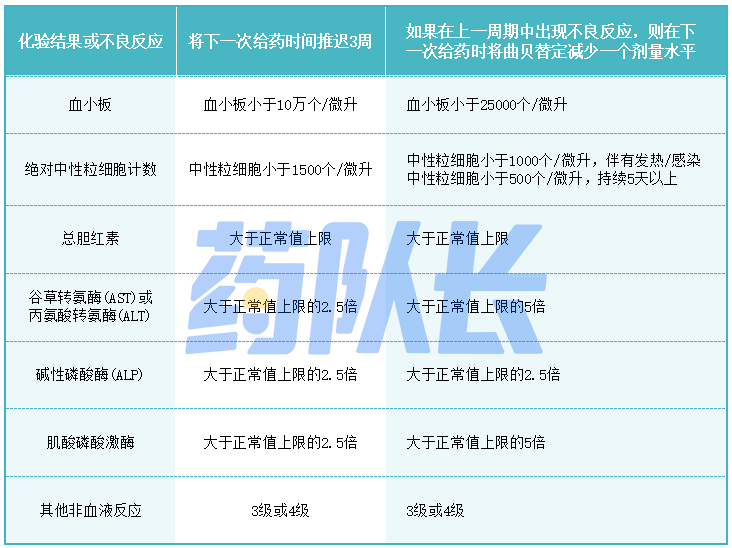
曲贝替定的推荐起始剂量和减量剂量见表2:
表2:推荐起始剂量和剂量减量
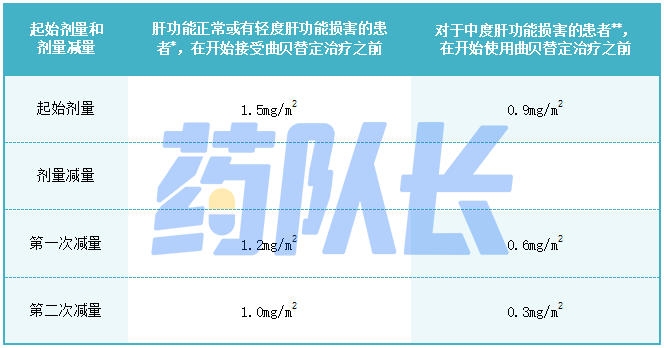
*包括胆红素大于正常值上限的1至1.5倍,以及任何谷草转氨酶或谷丙转氨酶的患者。
**包括胆红素水平高于正常值上限1.5倍至3倍,且谷草转氨酶和谷丙转氨酶低于正常值上限8倍的患者。
4.准备
曲贝替定是一种细胞毒性药物,请遵循适用的特殊处理和处置程序1。
(1)使用无菌技术将20mL注射用无菌水注入小瓶中,摇动小瓶直至完全溶解,重组溶液为无色或淡棕黄色的透明液体,含0.05mg/mL曲贝替定。
(2)在进一步稀释前检查是否有颗粒物和变色,如发现颗粒或变色,请丢弃小瓶。
(3)复溶后立即提取计算体积的曲贝替定,并用500mL0.9%氯化钠注射液或5%葡萄糖注射液进一步稀释,
切勿将曲贝替定与其他药物混合。
(4)重新配制冻干粉后30小时内,丢弃剩余溶液。
(5)曲贝替定稀释溶液与I型无色玻璃瓶、聚氯乙烯(PVC)和聚乙烯(PE)袋和管、聚乙烯(PE)和聚丙烯(PP)混合物袋、聚醚砜(PES)在线过滤器、钛、铂或塑料端口、硅胶和聚氨酯导管以及接触面由PVC、PE或PE/PP制成的泵兼容。
5.管理
(1)使用带有0.2微米聚醚砜(PES)在线过滤器的输液器,在24小时内通过中心静脉输注重新配制的稀释溶液,以降低接触溶液配制过程中可能引入的偶然病原体的风险。
(2)在初次复溶后30小时内完成输注,丢弃任何未使用的复溶的药物或输液。

- 【宫颈癌】ZG005[适 应 症]一线标准治疗失败的晚期宫颈癌[试验分期]Ⅰ期
- 【BRAF突变实体瘤】双机制ERK1/2抑制剂GH55[适 应 症]BRAF突变实体瘤[试验分期]Ⅰ期
- 实体瘤|KH801注射液[适 应 症]复发/难治性或转移性晚期实体瘤患者[试验分期]Ⅰ期
- 初治胃癌|CLDN18.2单抗ASKB589联合化疗+免疫治疗[适 应 症]不可切除的局部晚期、复发性或转移性胃及食管胃交界处腺癌[试验分期]Ⅲ期
- 弥漫大B细胞淋巴瘤|盐酸米托蒽醌脂质体[适 应 症]复发性/难治性弥漫大B细胞淋巴瘤[试验分期]Ⅱ期
- 宫颈癌|PD-1/TIGIT双抗ZG005[适 应 症]至少经一线标准治疗失败(既往需要接受过含铂方案的化疗)的复发转移性宫颈癌[试验分期]Ⅰ期、Ⅱ期